Anvisa analisa pedido da Pfizer para vacinar crianças entre 5 e 11 anos
A agencia reguladora informou que a vacina será diferente das doses aplicadas para crianças a partir dos 12 anos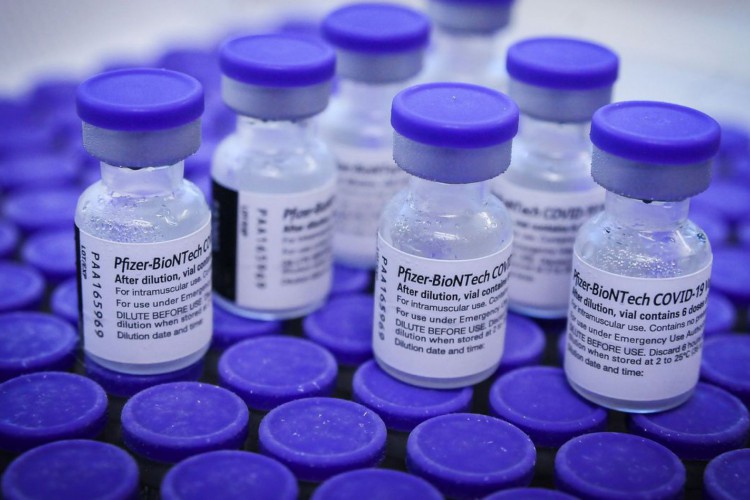
O consórcio Pfizer (BioNTech) entrou com o pedido de autorização juntamente à Agência Nacional de Vigilância Sanitária (Anvisa) para que sua vacina contra a Covid-19, a Comirnaty, possa ser aplicada em crianças com idades entre 5 e 11 anos.

A Anvisa terá até 30 dias para analisar a documentação e os estudos entregues pelas farmacêuticas e avaliar aspectos como segurança e eficácia do imunizante no público pretendido.
É + que streaming. É arte, cultura e história.
As farmacêuticas já haviam anunciado no mês passado que entrariam com a solicitação. A ampliação da imunização para esse público foi submetida e aprovada pela autoridade sanitária dos Estados Unidos (FDA, na sigla em inglês), em outubro.
Segundo informado pela Anvisa, a dose da vacina para crianças será diferente daquela utilizada para pessoas a partir de 12 anos. Os frascos também terão cores distintas para evitar erros na aplicação.
A vacina da Pfizer-BioNTech já havia obtido a autorização para aplicação em adolescentes, razão pela qual é a marca que vem sendo utilizada nesse público pelas autoridades de saúde no Brasil.
Tenha acesso a todos os colunistas. Assine O POVO+ clicando aqui
Dúvidas, Críticas e Sugestões? Fale com a gente
