Pfizer apresenta dados de sua vacina anticovid para crianças ao regulador dos EUA
Empresa planeja buscar aprovação formal "nas próximas semanas"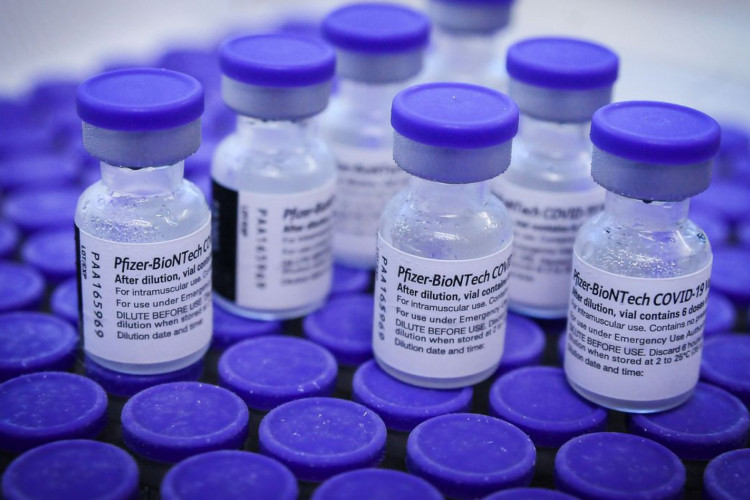
A aliança Pfizer/BioNTech anunciou nesta terça-feira (28) que apresentou os resultados de seus testes da vacina contra a Covid-19 em crianças de 5 a 11 anos para a agência de medicamentos dos EUA (FDA), e que planeja buscar aprovação formal "nas próximas semanas".
É + que streaming. É arte, cultura e história.
Os ensaios foram conduzidos em 2.300 crianças com idades entre 5 e 11 anos, e a dose foi ajustada para 10 microgramas versus 30 microgramas para os outros grupos etários.
Esses dados "foram submetidos à FDA para análise preliminar", indicou a Pfizer em um comunicado.
Leia Mais - Anvisa autoriza vacina da Pfizer para crianças a partir de 12 anos
"Espera-se que um pedido formal de autorização de emergência seja submetido nas próximas semanas", acrescentou a empresa.
No início deste mês, a FDA disse que uma vez que o pedido fosse submetido, iria "examinar os dados para avaliar os benefícios e riscos" e que completaria sua revisão "provavelmente em questão de semanas, não meses".
Muitos pais esperam que seus filhos tenham acesso às vacinas, especialmente no início do ano letivo e nas aulas presenciais.
Até agora, a vacina da Pfizer é totalmente permitida para maiores de 16 anos e autorização de emergência para aqueles entre 12 e 15 anos.

